Physique chimie : l'eau d'une piscine. Concours
CAPLP maths sciences 2025.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
Partie 2. Physique
chimie.
A.Qualité de l'eau d'une
piscine.
Un opérateur mesure
le pH de l'eau : pH = 6,5. Il décide de faire un traitement par apport
de carbonate de sodium.
1. Commenter cette
valeur.
L'eau est trop acide. Le pH doit être compris ente 6,9 et 7,7 selon la
législation.
2. Expliquer
pourquoi l'apport de carbonate de sodium est de nature à améliorer le
pH de l'eau.
L'ion carbonate est une base : elle va réagir avec l'excès d'ion H+aq.
3. Indiquer
l'impact prévisible de cet apport sur le titre alcalimétrique complet
(TAC) de l'eau.
L'apport d'ion carbonate et hydrogénocarbonate augmente la valeur du
TAC de l'eau.
Détermination
du TAC de l'eau.
On souhaite déterminer le TAC de l'eau dont le
pH a été ajusté à pH = 7,6.
On dose les ions HCO3- dans V=100,0 mL de
cette eau en présence de vert de bromocrésol par une solution d'acide
chlorhydrique de concentration CA = 2,0 10-2 mol
/ L. Le volume versé à l'équivalence vaut VE = 8,3 mL.
4. Montrer que l'ion HCO3-
prédomine à pH = 7,6.
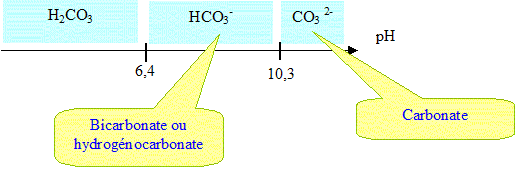
5. Expliquer
pourquoi l'ion hydrogénocarbonate est une espèce qualifiée d'amphotère.
Cet ion peut de comporter comme un acide ou comme une base.
6. Donner une
représentation de Lewis de cet ion.
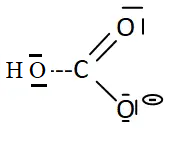 7. Écrire
l’équation de la réaction de titrage des ions hydrogénocarbonate et
calculer sa constante d’équilibre K. Conclure sur le caractère total de
la transformation.
7. Écrire
l’équation de la réaction de titrage des ions hydrogénocarbonate et
calculer sa constante d’équilibre K. Conclure sur le caractère total de
la transformation.
HCO3 -
aq +H3O+aq --> CO2aq + 2H2O(l).
K = [CO2aq] / ([HCO3 -
aq][H3O+aq]) ;
Ka = [CO32-aq] / ([HCO3 -
aq][H3O+aq]/) ; pKa =10,3 ; Ka = 10-10,3.
K = 1/ Ka = 1010,3.
K est très grand : la transformation est donc totale.
8. Expliquer précisément comment est
repérée l’équivalence du titrage.
Changement de couleur de l'indicateur coloré : passage du bleu au jaune.
9.
Déterminer la concentration en masse en ions hydrogénocarbonate. En
déduire, le TAC de l’eau de la piscine et conclure par rapport aux
valeurs recommandées.
A l'équivalence : CA VE = V C ; C = 0,020 * 8,3 /
100=0,00166 mo / L.
M(NaHCO3)=84 g / mol ; 0,00166 x84 ~0,14 g / L = 140 mg / L.
1°f = 12,2 mg d'ion HCO3- : TAC = 140 / 12,2
~11,5 °f, valeur comprise entre 8 et 12 °f.
L'eau est conforme...
Étude énergétique d’un
bassin « écologiquement raisonnable »
On s’intéresse dans cette partie à une étude énergétique d’un bassin
nordique. Il s’agit d’une piscine classique non couverte et peu
profonde afin de permettre le chauffage de l’eau sur un volume réduit,
dans le but d’être le plus économique possible. Il n’y a ni
déshumidification, ni chauffage de l’air ambiant comme c’est le cas
pour une piscine couverte.
B.1.1 – Pertes
énergétiques d’un bassin nordique par évaporation
La température de l’eau du bassin diminue à cause de différentes pertes
énergétiques. Ces pertes correspondent aux échanges thermiques qui ont
lieu entre l’eau et son milieu environnant (parois de la piscine, air
extérieur) et à l’évaporation en l’absence de couverture.
10. Citer et
décrire les trois modes de transfert thermique qui peuvent avoir lieu
sur le bassin nordique.
Conduction, convection et rayonnement.
11. Calculer le
volume d’eau perdu par évaporation par le bassin nordique sans
couverture sur une période de 24 heures. Commenter le résultat.
Pertes énergétiques par évaporation :
En journée (8 h -20 h): Qévap jour =2,0 MW h =7200 MJ .
La nuit ( 20 h- 8 h) : Qévap nuit =6,0 MW h= 6,0 x3600=21 600 MJ.
Total = 28 800 MJ.
Enthalpie massique de vaporisation de l'eau : Lv = 2,4 MJ kg-1.
Masse d'eau perdue : 21 600 / 2,4=12 000 kg.
Volume d'eau perdue 12 m3.
12. Expliquer
pourquoi le phénomène d’évaporation contribue au refroidissement de
l’eau du bassin. Déterminer la diminution journalière (24 heures) de la
température de l’eau qui résulterait de l’évaporation seule, en
l’absence de couverture et de tout autre transfert (notamment pas
d’apport d’eau et absence de chauffage et de tout autre type d’échange
thermique).
L'évaporation de l'eau nécessite un apport d'énergie fournie par l'eau
du bassin qui va donc se refroidir.
Enthalpie massique de vaporisation de l'eau : 2,4 MJ kg-1.
Energie perdue :Q = 2,4 x 12 000 =2,88 104 MJ.
Q = m c DT ;
Volume de la piscine :50 x 25 x1,5=1875 m3.
m = 1,875 106 kg. c = 4,2 103 J kg-1 K-1.
DT =2,88 1010 /
(1,875 106 x4,2 103)~3,7 K.
B.1.2 – Diminution des
pertes énergétiques par utilisation d’une couverture
Pour réduire les pertes énergétiques et éliminer pratiquement toutes
les pertes par évaporation, on installe une couverture en mousse de
polyéthylène sur l’eau lorsque le bassin n’est pas utilisé,
c’est-à-dire la nuit de 20 h à 8 h.
13. Donner la
formule semi-développée et le nom, dans la nomenclature officielle, du
monomère à l’origine de la synthèse du polyéthylène.
Ethylène H2C=CH2.
14. Déterminer le
degré de polymérisation 𝑛𝑛 d’un polyéthylène dont la masse molaire
est de 3,00 × 106 g ∙ mol−1.
M(éthylène) =28 g / mol.
3,00 106 / 28=1,07 105.
15. Calculer la
puissance thermique perdue à travers la couverture. Conclure sur
l’énergie économisée Q, en MW∙h, dans ces conditions en posant la
couverture sur le bassin pendant une période de 12 heures (la nuit de
20 h à 8 h).
e = 5,0
mm ; S =1250 m2 ; l
= 0,038 W m-1 K-1. Teau = 28°C ; Tair
nocturne = 10°C.
Résistance thermique R = e / (lS)
=5,0 10 -3 /(0,038 1250)=1,05 10-4 K W-1.
Puissance perdue = DT / R =(28-10) / (1,05 10-4)=1,71 105
W.
Energie 1,71 105 x12=2,05 106 Wh =2,05 MWh.
|
...
= =
|
....
|
B.2
– Étude du chauffage du bassin par utilisation des eaux usées
Il est nécessaire d’avoir un système de chauffage
pour compenser les pertes énergétiques du bassin et le maintenir à
température constante. Pour cela, il existe un procédé permettant
d’exploiter le potentiel thermique des eaux usées domestiques qui
transitent dans les réseaux urbains.
B.2.1 – Étude de
l’échangeur récupérateur de l’énergie thermique des eaux usées.
Le fluide caloporteur utilisé dans l’échangeur de récupération de
l’énergie des eaux usées est de l’eau glycolée. Cette eau contient du
glycol de formule semi-développée : HO − CH2 − CH2
− OH.
16. Nommer le
groupe caractéristique présent dans la molécule de glycol et donner la
fonction chimique associée.
Groupe OH hydroxyle ; fonction alcool primaire.
17. Déterminer la
puissance thermique récupérée par l’échangeur spiralé à partir des eaux
usées circulant dans le réseau d’assainissement .
Eaux usées : température à l'entrée de l'échangeur : 17 °C ;
température de sortie : 12 °C.
Débit volumique Dv=30 m3 h-1.
Q = Dv reau
c DT =30 x103
x4,2 103 x(17-12)=6,3 108 J= 6,3 108 /
3600=1,75 105 Wh.
Durée : 12 h ; puissance thermique récupérée :1,75 105
/12=1,46 104 W.
Dans l'échangeur : température d'entrée du fluide : 16°C ; température
de sortie : 10 °C.
B.2.2 – Étude de la pompe
à chaleur couplée à l’échangeur
18. Justifier que
la formule du COP de la pompe à chaleur permet de quantifier la
performance de la pompe à chaleur. Préciser et justifier les signes des
grandeurs Qf, Qc et W.
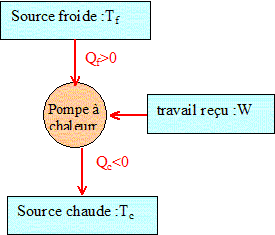
coefficient
d’efficacité , notée e, ( réversibilité) : gain / dépense =|
chaleur cédée à l'eau |divisée par le travail reçu.
e = -Qc /W.
19. Dans le cas
d’un fonctionnement réversible de la pompe à chaleur entre une source
froide à la
température Tf et une source chaude à la température Tc,
montrer que le coefficient de COPrév =TC / (TC-Tf)
COPrév = - Qc / W.
Premier principe de la thermodynamique :W+Qc+Qf=0.
COPrév = - Qc /(-Qc+Qf)= Qc
/(Qc-Qf)=TC / (TC-Tf).
20. Calculer le
coefficient COPrév pour Tf = 15 °C et Tc
= 50 °C.
COPrév =50 / (50-15)=1,4
Le constructeur annonce pour le fonctionnement réel de la pompe à
chaleur un COP égal à 4.
21. Commenter la
validité de l’hypothèse de réversibilité du fonctionnement de la pompe
à chaleur.
1,4 diffère de 4 : l’hypothèse de réversibilité du fonctionnement de la
pompe à chaleur n'est pas valide..
On considère que l’énergie thermique reçue par le fluide de la part de
la source froide pendant une heure est Qf=170 kW∙h.
22. En déduire
l’énergie thermique Qc produite par la pompe à chaleur et le
travail W à fournir au compresseur pendant une heure.
1,4 = Qc /(Qc-Qf) = Qc /(Qc-170)
.
1,4 Qc-1,4 *170 = Qc ; 0,4 Qc =238 ; Qc
=595 kWh.
23. Calculer le
coût annuel du chauffage de la piscine par le procédé étudié. Conclure
en comparant avec le coût annuel d’un chauffage au gaz de la piscine.
Prix du kWh d'électricité : 0,25 €.
595 x 0,25 x365=5,4 104 €= 54 k€.
Coût annuel d’un chauffage au gaz de la piscine : 190 k€.
Economie réalisée : 190-54=136 k€.
|
|
|
|