Les gaz dans l'organisme du plongeur. Concours
général 2026.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
Au cours de la plongée, des échanges gazeux ont lieu entre I'air respiré et le sang. Dans toute cette partie, on
considèrera seulement les deux gaz très majoritaires de l'air : le diazote et le dioxygène. Pour simplifier, leurs
proportions en quantité de matière dans I'air seront prises égales à 80 % pour le diazote, et 20 % pour le dioxygène.
Cette composition est supposée identique pour I'air dans la bouteille du plongeur.
Afin de quantifler la concentration d'un gaz noté A dans un mélange gazeux, on déflnit sa pression partielle PA :
c'est la pressiori qu'aurait ce gaz s'il était seul dans le même volume. La pression partielle est proportionnelle à
la pression totale P, c'est la loi de Dalton :
PA= xAP
où xA est la proportion en quantité de matière du gaz A dans le mélange.
Les gaz respirés passent dans le sang par l'intermédiaire des alvéoles pulmonaires et se dissolvent dans le liquide
sanguin au fur et à mesure de la plongée. Au bout d'une durée
suffisante, un équilibre s'établit, c'est l'équilibre de saturation.
Lorsque l'équilibre de saturation est établi pour le gaz A, sa pression partielle dans la phase gazeuse PA et sa
concentration en quantité de matière dans la phase liquide CA sont proportionnelles, c'est la loi de Henry:
PA= kHCA.
La constante kH est appelée constante de Henry. Elle dépend de la nature du gaz, du liquide, et de la température.
Ainsi, pour la dissolution des gaz dans le sang à 37 "C :
- dioxygèn e : kH O2, = 1,0 x 103 bar L. mol-1.
- diazote : kH N2, = 1,9 x 103 bar.L.mol-1.
Désaturation du diazote lors de la remontée
Tout au long de la plongée, afin que les poumons du plongeur ne soient
pas écrasés, la pression de l'air respiré doit rester identique à celle
de l'eau. Lors d'une descente en profondeur, la pression de l'eau
augmente et donc la pression partielle en diazote dans l'air respiré
augmente également : le diazote se dissout progressivement dans le sang
et finit par s'accumuler dans les tissus.
Dans l'eau, la pression extérieure évolue de manière affine avec la profondeur : elle augmente de 1,0 bar tous les 10 m.
Q42. En utilisant
la loi de Dalton, calculer la pression partielle en diazote dans l'air
respiré lorsque le plongeur est en surface, puis lorsqu'il est.à
la.profondeur h = 30 m.
A la surface : PN2 =0,80 x 1 = 0,80 bar.
A la profondeur h =30 m : PN2 =0,80 x 4 = 3,2 bar.
Les échanges gazeux et les équilibres de dissolution ne sont cependant pas instantanés : leur cinétique dépend
de la nature des tissus (muscle, graisse...). Les tables de plongée
usuelles sont celles de la Marine Nationale MN90, qui considèrent 12
types de tissus différents. Pour simplifier l'étude, on adopte le
modèle historique de Haldane, qui considère 5 tissus.
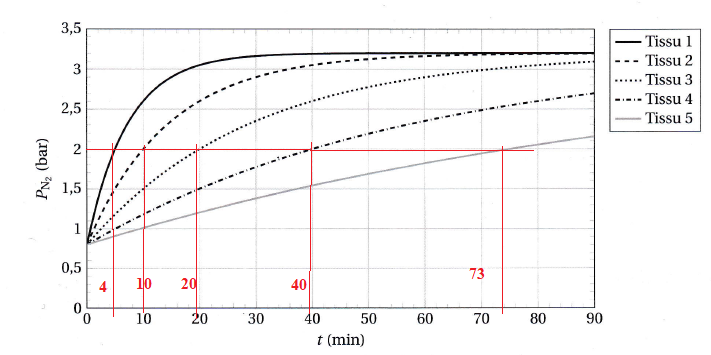
L'évolution temporelle de Ia pression partielle en diazote dans le
modèle de Haldane est représenté pour un plongeur, parti initialement
de la surface, et qui descend rapidement jusqu'à la profondeur h = 30 m.
Chaque tissu est caractérisé par sa période T, durée nécessaire pour
que l'augmentation de pression partielle en diazote soit effectuée à
50%.
Augmentation à 50 % : (3,2-0,8) / 2 =1,2 bar ; 1,2+0,8 = 2 bar.
Q43. Mesurer la période T de chacun des cinq tissus considérés.
Dans la suite, on considèrera un plongeur qui descend rapidement à la profondeur h = 30 m, y séjourne 30 min,
puis désire remonter en surface.
Lors de sa remontée, sous I'effet de la diminution de pression extérieure, le diazote s'élimine progressivement
des tissus, ce qui s'accompagne de la formation de bulles qui remontent Ie réseau veineux et qui doivent être
éliminées par les poumons. La formation de bulles n'entraîne pas nécessairement un accident ou une maladie
de "décompression", mais le risque augmente toutefois avec leur nombre et leur rayon.
Q44. Estimer le nombre de bulles de diamètre d = 8 µm (diamètre moyen des plus petits vaisseaux sanguins)
qui seraient formées une fois le plongeur remonté à la surface, à une température de 37°C sous pression atmosphérique.
On considérera pour simplifler seulement le tissu 1, avec un volume sanguin égal à Vsang = 5L.
Commenter le résultat obtenu.
Volume d'une bulle : 3,14 d2 /4 =3,14 x(8 10-6)2 /4 =5,0 10-11 m3 =5,0 10-8 L.
Pression du diazote dans le sang au bout de 30 min, tissu 1: P1=3,2 bar = 3,2 105 Pa.
A température constante : P1Vsang = Patm V2 ; V2 =3,2 105 x 5 / 105=16 L.
Nombre de bulles : 16 / (5,0 10-8)=3,2 108.
Le risque lié à la décompression est quantiflé par un coeficient de sursaturation, noté SC, déflni par la relation
suivante:
SC = PN2 0 /Pext
- PN2 0: pression partielle en diazote à la profondeur de départ,
- Pext : pression à l'extérieur atteinte après remontée. Pour une remontée en surface (à I'air libre) :
Pext= Patm =1 bar.
pour un arrêt à une profondeur intermédiaire, c'est la pression dans l'eau à cette profondeur.
La décompression reste sans risque tant que SC ne dépasse pas une valeur particulière dite "critique" SC" (voisine
de
2 dans tous les tissus). Dans le cas ou SC > SCc, le plongeur devra
s'arrêter en cours de remontée à une profondeur intermédiaire durant
une durée minimale : c'est le palier de décompression.
Q45. Calculer, pour chacun des tissus, la pression extérieure minimale à respecter pour éviter tout accident de
décompression lors de la remontée, après 30 min passées à h = 30 m de profondeur. Le coefficient de sursaturation
critique SC" sera pris égal à 2,0 pour chacun des tissus pour simplifier.
Tissu 1 : PN2 =3,2 bar ; Pext = 3,2 /2 =1,6 bar.
Tissu 2 : PN2 =2,9 bar ; Pext = 2,9 /2 =1,45 bar.
Tissu 3 : PN2 =2,35 bar ; Pext = 2,35 /2 =1,17 bar.
Tissu 4 : PN2 =1,8 bar ; Pext = 1,8 /2 =0,9 bar.
Tissu 5 : PN2 =1,4 bar ; Pext = 1,4 /2 =0,7 bar.
Q46. Déterminer alors la profondeur à laquelle le plongeur doit s'arrêter pour effectuer un palier de décompression,
arrondie au mètre près.
Palier de sécurité : arrêt de 3 min à 5 m.
Palier profond : arrêt de 30 à 50 s à 15 m.
|
...
= =
|
....
|
Fixation et transport du dioxygène dans le sang par l'hémoglobine
Contrairement au diazote, le dioxygène ne pose pas de problème majeur, car il ne s'accumule pas lors de la plongée
: il est üansporté par l'hémoglobine, protéine contenue dans les
globules rouges du sang, et est consommé au niveau des organes et des
muscles pour la respiration.
Une protéine est un biopolyrnère, constitué de monomères de chaînes
latérales variables. Chaque paire de monomères est associée par une
liaison covalente, appelée liaison peptidique, dont la formation est
exposée :

Q47. Nommer la famille de molécules constituant les monomères des protéines, et la famille fonctionnelle correspondant
à la liaison peptidique.
Monomère : acide a aminé.
Protéine : polypeptide.
La molécule d'hémoglobine non oxygénée possède quatre sites, appelés
hèmes, pouvant fixer chacun une molécule de dioxygène grâce à un cation
fer et une molécule d'histidine incluse dans la chaine protéique.
Q48. Représenter le schéma de Lewis d'une molécule de dioxygène.
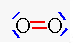
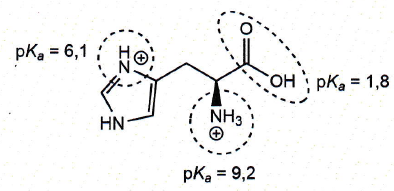
La structure de l'histidine libre est représentée ci-dessous sous sa
forme totalement protonée. L'lhistidine possède en effet trois groupes
avec des propriétés acido-basiques, qui sont entourés et dont la valeur
des pKa des couples correspondants est indiquée. Le pH sanguin est
proche de 7,4.
Q49. Dresser le
diagramme de prédominance acido-basique de l'histidine libre en
solution aqueuse, en représentant les différentes formes rencontrées.
Préciser quelle serait la forme prédominante de l'histidine si elle
était libre dans le sang.
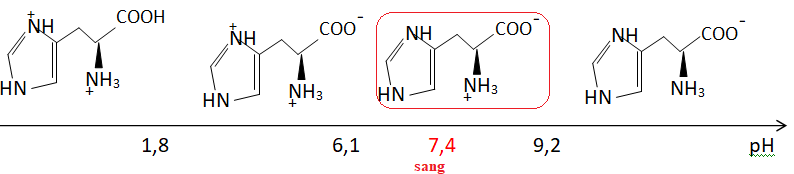
Q50. Pour un
fragment histidine inclus dans la chaîne protéique de l'hémoglobine du
sang, préciser si son cycle azoté est chargé ou non.
A pH = 7,4, le cycle azoté de l'histidine n'est pas chargé.
Q51. Nommer l'interaction entre l'histidine et la molécule de dioxygène, représentée en pointillés.
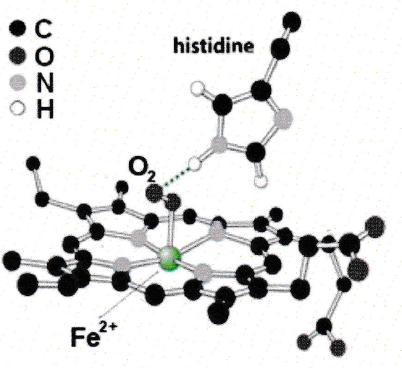
Liaison covalente de coordination..
Équilibre de fixation du dioxygène par l'hémoglobine
Le taux de saturation Y de l'hémoglobine est déflni comme la proportion
de sites ayant fixé du dioxygène. Des mesures, effectuées à 37'C et à
pH =7,4, ont permis de tracer l'évolution du taux de saturation Y (en
%) en fonction de la pression partielle en dioxygène.
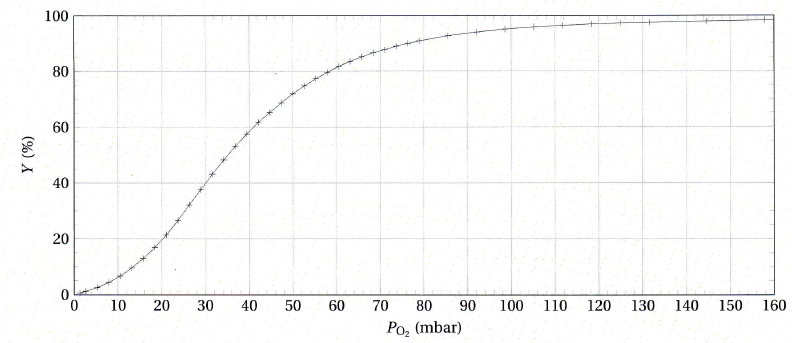
La pression partielle en dioxygène au niveau des poumons est en moyenne
de 130 mbar, alors que celle au niveau des muscles est de 30 mbar.
Q52. Déterminer la fraction en dioxygène capté au niveau des poumons que l'hémoglobine libère au niveau des muscles.
(130-30) /130 ~0,77 ( 77 %).
L'hémoglobine est en moyenne à une concentration en masse dans le sang de 160 g / L.
Q53. Calculer la concentration en quantité de matière moyenne en dioxygène fixé à l'hémoglobine du sang au niveau des poumons.
160 x 160 / 30 =850 g / L.
Q54. Calculer la
concentration qui serait observée en absence d'hémoglobine, c'est à
dire en tenant compte seulement de la dissolution dans le sang au
niveau des poumons. Commenter
130g / L ; 850 /130 ~6,5 fois plus faible.
On note :
Hb :forme non oxygénée de l'hémoglobine.
Hb(O2)n : forme partiellement oxygénée avec n le nombre moyen de molécules de dioxygène fixées par molécule d'hémoglobine.
Q55. Dans quel intervalle se situe n ?
Une molécule d'hémoglobine peut fixer 4 molécules d'oxygène grâce à ses 4 groupements hème.
n se situe entre 1 et 4.
Le modèle de Hill considère un unique équilibre de dissociation de l'hémoglobine oxygénée sous la forme suivante :
Hb(O2)n aq = Hb(aq) + nO2aq. Constante thermodynamique notée K.
Le taux de saturation de l'hémoglobine s'exprime par : Y = [Hb(O2)n]éq / ([Hb(O2)n]éq+ [Hbéq]).
Q56. En supposant que l'équilibre de dissociation est établi, montrer la relation suivante :
(1-Y) / Y =K(c° /[O2]éq)n avec c° = 1 mol / L.
K = [Hbéq][O2]éq)n /(c°[Hb(O2)n]éq ).
1 / Y = ([Hb(O2)n]éq+ [Hbéq]) / [Hb(O2)n]éq = 1 + [Hbéq]) / [Hb(O2)n]éq ;
1 / Y -1= [Hbéq]) / [Hb(O2)n]éq = K c°/ [O2]éq)n .
Q57. En déduire que la relation précédente peut se mettre sous la forme : log(Y / (1-Y) = pKD +n log(PO2).
log(Y / (1-Y) =-log((1-Y) / Y) =- log K -log ([O2]éq)n/ c°)= pKD -n log ([O2]éq/ c°).
log(Y / (1-Y) = pKD +n log(PO2).
Exprimer la constante pKD en fonction de K, n, c° et de la constante de Henry du dioxygène kH, O2.
K = ([O2]éqn (1-Y) / (Y c°).
PO2= kH,O2 [O2]éq. ;
PO2n= knH,O2 [O2]néq =knH,O2 K c° Y /(1-Y).
log
PO2n=log knH,O2 + log (Kc°) +log(Y/(1-Y)).
log
PO2n=log knH,O2 + log (Kc°) +pKD +n log(PO2).
0=log knH,O2 + log (Kc°) +pKD .
pKD =-log knH,O2 - log (Kc°).
La représentation graphique de log(Y / (1-Y)) en fonction de log (PO2) est appelée courbe de Hill.
Q58. Préciser l'allure attendue pour cette courbe.
La fonction logarithme est croissante à partir de pKD.
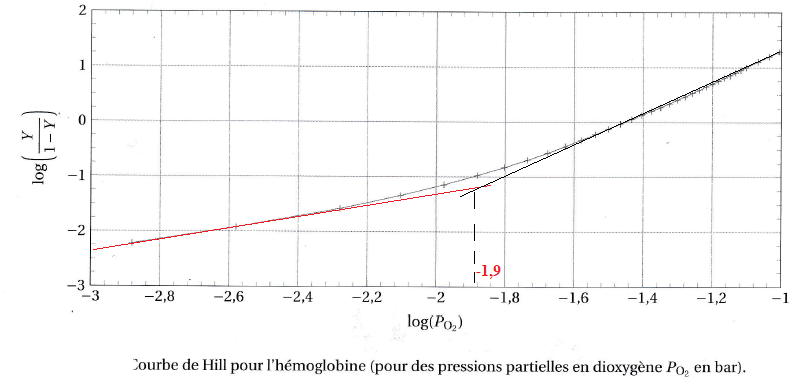
La courbe de Hill expérimentale peut être ici approximativement
décomposée en deux portions affrnes, correspondant respectivement aux
domaines de basse et haute pression partielle en dioxygène.
Q59. Déterminer graphiquement une estimation de la valeur de log(PO2) délimitant les deux domaines.
log(PO2) = -1,9.
Q60. La valeur de n dans le domaine des basses pressions est approximativement de 1. Déterminer graphiquement la valeur de pKD puis celle de KD dans ce domaine.
log(Y / (1-Y) = pKD + log(PO2) ; pKD = log(Y / (1-Y) -log(PO2).
Au point de coordonnée (-2,75 ; -2) : pKD =-2+2,75= 0,75.
KD = 10-0,75 = 0,18.
Q6l. Déterminer graphiquement la valeur de n dans le domaine des hautes pressions, puis la valeur de KD.
n : pente de la droite =1,8 /0,6 = 3.
log(Y / (1-Y) = pKD + log(PO2) ; pKD = log(Y / (1-Y) -log(PO2).
Au point de coordonnée (-1 ; 1,3) : log(Y / (1-Y) = pKD +n log(PO2).
1,3= pKD +3 *(-1) ; pKD =4,3 ;
4,3 = -log(KD) ; KD= 10-4,3 =5 10-5.
Q62. Comparer les
valeurs de n.obtenues aux domaines de basses et hautes pressions et
commenter en lien avec l'efficacité du transport de dioxygène par
l'hémoglobine entre les poumons et les muscles.
Aux basses pressions, n=1 ; aux hautes pressions n = 3 : dans les
poumons l'hémoglobine se sature en oxygène. Dans les muscles
l'hémoglobine libère une partie de l'oxygène ce ui est indispensable
pour l'approvisionnement des cellules.
Q63. Calculer la
valeur de la constante K pour chacun des deux domaines, et déterminer
comment évolue l'affinité de l'hémoglobine pour le dioxygène suivant la
teneur du milieu en dioxygène.
Q64. Expliquer
pourquoi le modèle de Hill, considérant un unique équilibre de fixation
du dioxygène, n'est pas totalement suffisant pour rendre compte des
observations expérimentales.
|
|
|
|